2º f - Física - 20/07
A 24/07
Até meados do século XIX, acreditava-se ser possível a construção
de uma máquina térmica ideal, que seria capaz de transformar toda a energia
fornecida em trabalho, obtendo um rendimento total (100%).
Para
demonstrar que não seria possível, o engenheiro francês Nicolas Carnot
(1796-1832) propôs uma máquina térmica teórica que se comportava como uma
máquina de rendimento total, estabelecendo um ciclo de rendimento máximo, que
mais tarde passou a ser chamado Ciclo de Carnot.
As máquinas térmicas são dispositivos que funcionam de acordo com o que estabelece a segunda lei da Termodinâmica:
“O calor não pode passar de forma espontânea de um corpo de menor temperatura para outro de temperatura mais alta.”
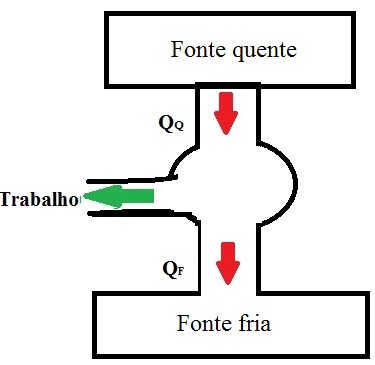
Sendo assim, as máquinas térmicas operam em ciclos, retirando uma quantidade calor (QQ) de uma fonte quente, convertendo parte desse calor em trabalho mecânico (τ) e rejeitando outra quantidade de calor para uma fonte fria (QF).
Esse esquema de funcionamento pode ser observado na figura a seguir:
Este ciclo seria composto de quatro processos, independente da substância:
- Uma expansão isotérmica reversível. O sistema recebe uma quantidade de calor da fonte de aquecimento (L-M)
- Uma expansão adiabática reversível. O sistema não troca calor com as fontes térmicas (M-N)
- Uma compressão isotérmica reversível. O sistema cede calor para a fonte de resfriamento (N-O)
- Uma compressão adiabática reversível. O sistema não troca calor com as fontes térmicas (O-L)
Obs.: A transformação adiabática ocorre quando um gás sofre expansão ou compressão muito rapidamente, sem que haja tempo suficiente para transferências de calor. Transformações adiabáticas são processos termodinâmicos nos quais não ocorrem transferências de calor entre um sistema e suas vizinhanças.
Numa máquina de Carnot, a quantidade de calor que é fornecida pela fonte de aquecimento e a quantidade cedida à fonte de resfriamento são proporcionais às suas temperaturas absolutas, assim:
Assim, o rendimento de uma máquina de Carnot é:
Logo:
Sendo:
Com isto se conclui que para que haja 100% de rendimento, todo o calor vindo da fonte de aquecimento deverá ser transformado em trabalho, pois a temperatura absoluta da fonte de resfriamento deverá ser 0K.
Partindo daí conclui-se que o zero absoluto não é possível para um sistema físico.
Exemplo:
Qual o rendimento máximo teórico de uma máquina à vapor, cujo fluido entra a 560ºC e abandona o ciclo a 200ºC?

Exercícios
1. Uma máquina que opera em ciclo de Carnot tem a temperatura de sua fonte quente igual a 330°C e fonte fria à 10°C. Qual é o rendimento dessa máquina?
2. Uma máquina térmica opera em ciclos retirando calor Q1 = 300 J de uma fonte térmica quente, T1 = 600 K, e rejeitando Q2 = 200 J em uma fonte fria T2 = 300 K, a cada ciclo, em que a diferença entre esses valores corresponde ao trabalho produzido por ciclo. Dado que as únicas trocas de calor da substância de trabalho da máquina com as fontes externas são essas duas descritas acima, qual é o rendimento térmico da máquina?
3. Uma máquina térmica tem rendimento de 40% e realiza um trabalho de 2000 Joules. Qual a quantidade de calor rejeitada para a fonte fria, em Joules, pela referida máquina?
4. Uma máquina de Carnot opera entre as temperaturas TQ = 900 K e TF = 400 K, sendo TQ a temperatura da fonte quente e TF a temperatura da fonte fria. A máquina realiza 800 J de trabalho em cada ciclo.
Com base nesse caso hipotético, qual a energia liberada em forma de calor, em Joule, para a fonte fria a cada ciclo?
Nenhum comentário:
Postar um comentário