O Átomo
Todas as substâncias são formadas de pequenas partículas
chamadas átomos. Para se ter uma ideia, eles são tão pequenos que uma cabeça de
alfinete pode conter 60 milhões deles.
Os gregos antigos foram os primeiros a saber que a matéria é
formada por tais partículas, as quais chamaram átomo, que significa
indivisível. Os átomos porém são compostos de partículas menores: os prótons,
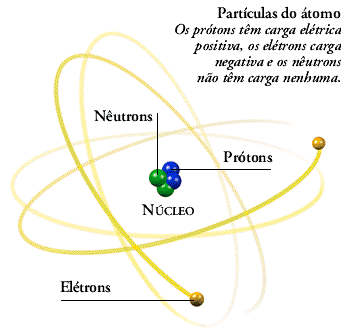
os nêutrons e os elétrons. No átomo, os elétrons orbitam no núcleo, que contém
prótons e nêutrons.
Elétrons são minúsculas partículas que vagueiam
aleatoriamente ao redor do núcleo central do átomo, sua massa é cerca de 1840
vezes menor que a do Núcleo. Prótons e nêutrons são as partículas localizadas
no interior do núcleo, elas contém a maior parte da massa do átomo.
No centro de um átomo está o seu núcleo, que apesar de
pequeno, contém quase toda a massa do átomo. Os prótons e os nêutrons são as
partículas nele encontradas, cada um com uma massa atômica unitária.
O Número de prótons no núcleo estabelece o número atômico do
elemento químico e, o número de prótons somado ao número de nêutrons é o número
de massa atômica. Os elétrons ficam fora do núcleo e tem pequena massa.
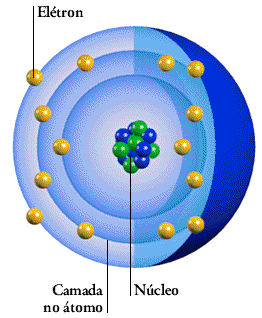
Há no máximo sete camadas em torno do núcleo e nelas estão
os elétrons que orbitam o núcleo. Cada camada pode conter um número limitado de
elétrons fixado em 8 elétrons por camada.
Características das Partículas:
Prótons: tem carga elétrica positiva e uma massa unitária.
Nêutrons: não tem carga elétrica mas tem massa unitária.
Elétrons: tem carga elétrica negativa e quase não possuem
massa.
Estudo do Átomo
Em 1911 o físico neozelandês Ernest Rutherford fez sua
"experiência da dispersão" para suas novas descobertas sobre a estrutura
do átomo e dela surgiu a base para o modelo de átomo que estudamos até os dias
de hoje.
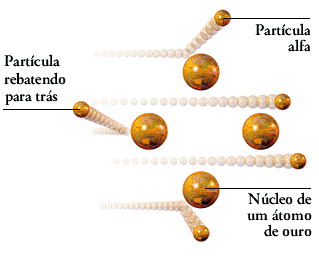
Rutherford bombardeou uma fina camada de ouro com partículas
alfa (partículas atômicas emitidas por alguns átomos radioativos), sendo que a
maioria atravessou a lâmina, outras mudaram ligeiramente de direção e algumas
rebateram para trás. Ele concluiu que isso acontecia porque em cada átomo de
ouro há um denso núcleo que bloqueia a passagem de algumas partículas.
Veja no simulador
https://phet.colorado.edu/sims/html/rutherford-scattering/latest/rutherford-scattering_pt_BR.html
1. (PUC) Uma importante contribuição do modelo de Rutherford foi
considerar o átomo constituído de:
a) elétrons mergulhados numa massa homogênea de carga positiva.
b) uma estrutura altamente compactada de prótons e elétrons.
c) um núcleo de massa desprezível comparada com a massa dos
elétrons.
d) uma região central com carga negativa chamada núcleo.
e) um núcleo muito pequeno de carga positiva, cercada por
elétrons.
2.O experimento de Rutherford consistia em bombardear uma fina
lâmina de ouro (0,0001 cm de espessura) com partículas alfa (α) emitidas pelo polônio (Po).
Muitas partículas atravessavam a lâmina de ouro sem sofrer desvio, e poucas
sofriam desvio. De acordo com esse princípio, assinale (V) ou (F) para as
sentenças a seguir:
( ) As partículas alfa emitidas possuíam carga
elétrica negativa.
( ) O elemento Polônio é radioativo.
( ) O tamanho do átomo é cerca de 10000 a 100000 vezes
menor que o seu núcleo.
3. Relacione os resultados do experimento com a lâmina de ouro às
conclusões tiradas por Rutherford:
I. Poucas partículas α não atravessavam a lâmina e voltavam.
II. A maior parte das partículasα atravessava a lâmina de ouro sem sofrer desvios.
III. Algumas partículas α sofriam desvios de trajetória ao atravessar a lâmina.
( ) o átomo possui um enorme espaço vazio
(eletrosfera), maior que o núcleo, onde os elétrons devem estar localizados.
( ) o núcleo do átomo é positivo, pois provoca uma
repulsão nas partículas α (positivas).
( ) existe no átomo uma pequena região onde está
concentrada sua massa (o núcleo).
4. As afirmativas a seguir são relacionadas à eletrosfera proposta
por Rutherford, assinale a que estiver INCORRETA:
a) região que apresenta carga negativa.
b) região praticamente sem massa.
c) região de menor proporção do átomo.
d) região que envolve o núcleo do átomo.
e) região onde se localizam os elétrons.
Nenhum comentário:
Postar um comentário