SÍMBOLOS DOS
ELEMENTOS QUÍMICOS
Os códigos básicos dos símbolos que adotamos
atualmente foram organizados no início do século XIX pelo químico sueco Jons
Jakob Berzelius. Adotou o latim como idioma principal para os símbolos.
Segundo a IUPAC (International Union of Pure and
Applied Chemistry - União Internacional de Química Pura e Aplicada), o símbolo de um elemento químico
é formado pela letra inicial maiúscula de seu nome em latim ou em grego. Quando
a letra inicial for a mesma nos nomes de vários elementos, utiliza-se uma
segunda letra, sempre minúscula:
Exemplos:
Carbono : C
Cálcio : Ca
Cádmio: Cd
Cloro: Cl
Outros
exemplos, são observados na tabela seguinte.
Observe a
tabela dos elementos químicos, com símbolo, nome, número atômico (Z) e massa
atômica (A):
Z
|
A
|
Elemento
|
Símbolo
|
Z
|
A
|
Elemento
|
Símbolo
|
Z
|
A
|
Elemento
|
Símbolo
|
1
|
1
|
Hidrogênio
|
H
|
38
|
87,6
|
Estrôncio
|
Sr
|
75
|
186
|
Rênio
|
Re
|
2
|
4
|
Hélio
|
He
|
39
|
89
|
Ítrio
|
Y
|
76
|
190
|
Ósmio
|
Os
|
3
|
7
|
Lítio
|
Li
|
40
|
91
|
Zircônio
|
Zr
|
77
|
191
|
Irídio
|
Ir
|
4
|
9
|
Berílio
|
Be
|
41
|
93
|
Nióbio
|
Nb
|
78
|
195
|
Platina
|
Pt
|
5
|
11
|
Boro
|
Br
|
42
|
96
|
Molibdênio
|
Mo
|
79
|
197
|
Ouro
|
Au
|
6
|
12
|
Carbono
|
C
|
43
|
99
|
Tecnécio
|
Tc
|
80
|
201
|
Mercúrio
|
Hg
|
7
|
14
|
Nitrogênio
|
N
|
44
|
101
|
Rutênio
|
Ru
|
81
|
204
|
Tálio
|
Tl
|
8
|
16
|
Oxigênio
|
O
|
45
|
103
|
Ródio
|
Rh
|
82
|
207
|
Chumbo
|
Pb
|
9
|
19
|
Flúor
|
F
|
46
|
106
|
Paládio
|
Pb
|
83
|
209
|
Bismuto
|
Bi
|
10
|
20
|
Neônio
|
Ne
|
47
|
108
|
Prata
|
Ag
|
84
|
209
|
Polônio
|
Po
|
11
|
23
|
Sódio
|
Na
|
48
|
112
|
Cádmio
|
Cd
|
85
|
210
|
Astato
|
At
|
12
|
24,3
|
Magnésio
|
Mg
|
49
|
115
|
Índio
|
In
|
86
|
222
|
Radônio
|
Rn
|
13
|
27
|
Alumínio
|
Al
|
50
|
119
|
Estanho
|
Sn
|
87
|
223
|
Frâncio
|
Fr
|
14
|
28
|
Silício
|
Si
|
51
|
122
|
Antimônio
|
Sb
|
88
|
226
|
Rádio
|
Ra
|
15
|
31
|
Fósforo
|
P
|
52
|
128
|
Telúrio
|
Te
|
89
|
227
|
Actínio
|
Ac
|
16
|
32
|
Enxofre
|
S
|
53
|
127
|
Iodo
|
I
|
90
|
232
|
Tório
|
Th
|
17
|
35,5
|
Cloro
|
Cl
|
54
|
131
|
Xenônio
|
Xe
|
91
|
231
|
Protactínio
|
Pa
|
18
|
40
|
Argônio
|
Ar
|
55
|
133
|
Césio
|
Cs
|
92
|
238
|
Urânio
|
U
|
19
|
39
|
Potássio
|
Kr
|
56
|
137
|
Bário
|
Ba
|
93
|
237
|
Netúnio
|
Np
|
20
|
40
|
Cácio
|
Ca
|
57
|
139
|
Lantânio
|
La
|
94
|
244
|
Plutônio
|
Pu
|
21
|
45
|
Escândio
|
Sc
|
58
|
140
|
Cério
|
Ce
|
95
|
243
|
Amerício
|
Am
|
22
|
48
|
Titânio
|
Ti
|
59
|
141
|
Praseodímio
|
Pr
|
96
|
247
|
Cúrio
|
Cm
|
23
|
51
|
Vanádio
|
V
|
60
|
144
|
Neodímio
|
Nd
|
97
|
247
|
Berquélio
|
Bk
|
24
|
52
|
Cromo
|
Cr
|
61
|
145
|
Promécio
|
Pm
|
98
|
251
|
Califónio
|
Cf
|
25
|
54,9
|
Manganês
|
Mn
|
62
|
150
|
Samário
|
Sm
|
99
|
252
|
Einstênio
|
Es
|
26
|
56
|
Ferro
|
Fe
|
63
|
152
|
Európio
|
Eu
|
100
|
257
|
Férmio
|
Fm
|
27
|
59
|
Cobalto
|
Co
|
64
|
157
|
Gadolínio
|
Gd
|
101
|
258
|
Mendelévio
|
Md
|
28
|
58,7
|
Níquel
|
Ni
|
65
|
159
|
Térbio
|
Tb
|
102
|
259
|
Nobélio
|
No
|
29
|
63,5
|
Cobre
|
Cu
|
66
|
163
|
Disprósio
|
Dy
|
103
|
262
|
Laurêncio
|
Lr
|
30
|
65,4
|
Zinco
|
Zn
|
67
|
165
|
Hólmio
|
Ho
|
104
|
261
|
Rutherfórdio
|
Rf
|
31
|
69,7
|
Gálio
|
Ga
|
68
|
167
|
Érbio
|
Er
|
105
|
262
|
Dúbnio
|
Db
|
32
|
72,6
|
Germânio
|
Ge
|
69
|
169
|
Túlio
|
Tn
|
106
|
266
|
Seabórgio
|
Sg
|
33
|
75
|
Arsênio
|
As
|
70
|
173
|
Itérbio
|
Yb
|
107
|
264
|
Bóhrio
|
Bh
|
34
|
79
|
Selênio
|
Se
|
71
|
175
|
Lutécio
|
Lu
|
108
|
269
|
Hássio
|
Hs
|
35
|
80
|
Bromo
|
Br
|
72
|
178
|
Háfnio
|
Hf
|
109
|
268
|
Meitnério
|
Mt
|
36
|
84
|
Criptônio
|
Kr
|
73
|
181
|
Tântalo
|
Ta
|
110
|
269
|
Darmstadtio
|
Ds
|
37
|
85,5
|
Rubídio
|
Rb
|
74
|
184
|
Tungstênio
|
W
|
Observamos, porém que existem alguns elementos que a regra não contempla,
ou seja, o símbolo não condiz com o nome do elemento, é o caso do Chumbo (Pb) - foi sugerido por
Berzelius, que adotou o
latim com idioma principal para os símbolos. Veja alguns exemplos na
tabela abaixo:
EXCEÇÕES NO SÍMBOLO
|
||
Elemento químico
|
Nome em latim
|
Símbolo
|
Fósforo
|
Phosphorum
|
P
|
Potássio
|
Kalium
|
K
|
Sódio
|
Natrium
|
Na
|
Cobre
|
Cuprum
|
Cu
|
Prata
|
Argentum
|
Ag
|
Ouro
|
Aurum
|
Au
|
Chumbo
|
Plumbum
|
Pb
|
Antimônio
|
Stibium
|
Sb
|
Mercúrio
|
Hydrargyrum
|
Hg
|
Estanho
|
Stannum
|
Sn
|
Para identificar um elemento químico
fora da Tabela Periódica, costuma-se colocar o símbolo do elemento no centro,
número de massa (A) na parte superior e o número atômico (Z) na parte inferior.
A figura abaixo mostra como isso pode ser feito para representar um elemento
químico:
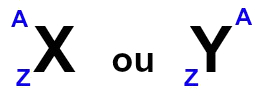
Essa
representação está de acordo com as normas da União da Química Pura e Aplicada
(IUPAC). A seguir temos os elementos químicos sódio (Na) e cloro (Cl) sendo
representados dessa forma:

Representação dos elementos sódio e cloro
Assim, o número atômico 11
identifica os átomos de sódio e o número atômico 17 identifica os átomos de
cloro.
Na tabela abaixo estão relacionados, alguns exemplos
de ocorrências naturais dos principais elementos químicos, com porcentagens
em massa:
Crosta terrestre ou litosfera
|
Hidrosfera
|
Atmosfera
|
Terra (globo)
|
Meteoritos
|
Estrelas
|
Corpo humano
|
O (50%)
|
O (85%)
|
N (75%)
|
Fe (40%)
|
Fe (40%)
|
H
|
O (65%)
|
Si (25%)
|
H (10%)
|
O (23%)
|
O (25%)
|
O (10%)
|
He
|
C (18%)
|
Al (7,5%)
|
Cl (2%)
|
Ar (1,5%)
|
Si (15%)
|
Ni (7%)
|
C
|
H (10%)
|
Fe (4,5%)
|
Na (1%)
|
H (0,02%)
|
Mg (8%)
|
Si (3%)
|
O
|
N (3%)
|
Ca (3,5%)
|
Mg (0,1%)
|
C (0,01%)
|
Ni (4%)
|
Mg (4%)
|
Si
|
P (1%)
|
Na (2,6%)
|
Ca (2,5%)
|
S (2,5%)
|
N
|
|||
K (2,4%)
|
Al (2%)
|
B
|
||||
Mg (2%)
|
S (0,5%)
|
Ne
|
Exercícios
1. (ACAFE-SC) O aumento da população mundial, que ocorreu
ao longo da história da humanidade, obrigou os agricultores a incrementarem a
produção de alimentos. Para tanto, além de outros recursos, são adicionados
milhões de toneladas de fertilizantes no solo, os quais apresentam na sua
composição N, P e K. Assinale a alternativa que apresenta elementos que fazem
parte da fórmula molecular dos principais fertilizantes.
a) nitrogênio - fósforo -
potássio
b) nitrogênio - água - argônio
c) nitrogênio - fósforo - mercúrio
d) fósforo - potássio -
mercúrio
e) água - magnésio – ozônio
2. O mercúrio foi responsável pela poluição de alguns
rios brasileiros em virtude de sua utilização no garimpo de ouro. Sua sigla é:
a) Mg
b) K
c) Sb
d) Hg
e) At
3. (UFAC) Os organismos vivos são constituídos de
compostos de carbono. Isto acontece devido às propriedades deste elemento.
Assim, um escritor de ficção científica pediu auxílio a um estudante do ensino
médio para a escolha de um elemento químico capaz de substituir o carbono na
formação de compostos. O estudante escolheu, com base em seus conhecimentos de
tabela periódica, um elemento que tem quase o mesmo tamanho do carbono,
eletronegatividade muito semelhante e mesma valência. O elemento escolhido,
número atômico igual a 14, foi:
a) nitrogênio
b) boro
c) alumínio
d) silício
e) fósforo
4. Dê as fórmulas das substâncias simples abaixo, sabendo que todas
são formadas por moléculas biatômicas.
Substância simples
|
Fórmula
|
Hidrogênio
|
|
Nitrogênio
|
|
Flúor
|
|
Cloro
|
Nenhum comentário:
Postar um comentário